Enfermedad de Dupuytren
Antecedentes
La contractura de Dupuytren es una enfermedad fibroproliferativa de la fascia palmar, capaz de producir una contractura en flexión de uno o más dedos, de naturaleza progresiva e irreversible.
Pertenece a un grupo de enfermedades llamadas fibromatosis, entre las que se incluyen:
- Fibromatosis plantar (enfermedad de Ledderhose)
- Fibromatosis del pene (enfermedad de Peyronie)
- Fibromatosis dorsal de las articulaciones interfalángicas proximales (nódulos de Garrod o almohadillas de nudillo)
Se caracteriza por el desarrollo de contractura debido a la formación de nódulos y cuerdas en la mano y los dedos. Los nódulos representan sitios de contracción activa de los tejidos. Las cuerdas están hechas de fascia normal que conectan los nódulos con la piel y otros tejidos.
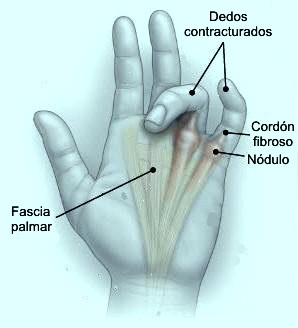
Anatomía
La fascia palmar es una lámina fibrosa triangular situada bajo el tejido celular subcutáneo de la palma. Tiene un doble papel: estabiliza los metacarpianos y fija la piel a las estructuras profundas. Algunas fibras transversales actúan como retináculo de los tendones flexores.
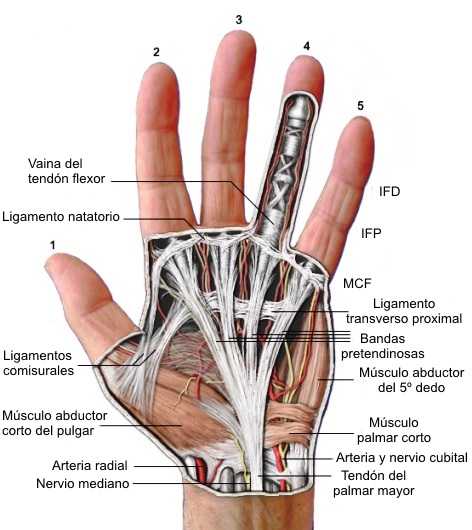
Sus fibras se organizan en tres planos: longitudinales, transversales y verticales. Las fibras longitudinales, provenientes del tendón del palmar largo, forman las bandas pretendinosas sobre los tendones flexores y son las más afectadas en la contractura de Dupuytren. En la palma distal se dividen en capas:
- Superficial: se inserta en la dermis distal a la articulación MCF, afectada en las picaduras cutáneas.
- Intermedia: se dirige a la lámina digital lateral, generando cuerdas en espiral.
- Profunda: rodea la vaina del tendón flexor, conectando con estructuras profundas.
Las fibras transversales forman el ligamento transversal superficial y el ligamento natatorio, ambos conectan la fascia con la piel y estructuras profundas. Las fibras verticales (septos de Legueu y Juvara) delimitan compartimentos fibroóseos y fijan la fascia a la dermis y placas palmares, limitando la movilidad cutánea.
En la zona palmo-digital distal, las bandas pretendinosas se bifurcan rodeando el tendón flexor y conforman la banda espiral de Gosset. Junto a la membrana intertendinosa, se integran con la lámina fascial lateral digital.
En los dedos, algunas fibras fasciales forman estructuras circulares que rodean el aparato osteotendinoso y separan el paquete neurovascular.
Los ligamentos de sostén del aparato extensor (triangular, sagital, retinacular transverso y oblicuo de Landsmeer) y los ligamentos cutáneos (natatorio, de Grayson, de Cleland) estabilizan el paquete neurovascular y transmiten tensión entre piel y tejido profundo.
Grayson: conecta la piel palmar con la vaina flexora, pasando por delante del paquete neurovascular.
Cleland: discurre dorsal al paquete neurovascular, uniendo hueso a dermis, con orificios vasculares.
Lámina fascial lateral digital: compuesta por fibras de la fascia superficial, ligamento natatorio y banda espiral.
Fascia retrovascular de Thomine: banda longitudinal entre el ligamento de Cleland y el paquete neurovascular, conectada con estructuras profundas.
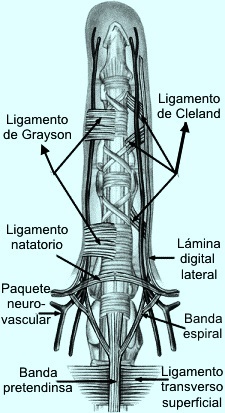
Los elementos fasciales superficiales más implicados en la enfermedad de Dupuytren son:
- Banda pretendinosa
- Banda espiral
- Lámina digital lateral
- Ligamento de Grayson
- Ligamento natatorio
Solo los ligamentos de Cleland y de Landsmeer permanecen indemnes.
Anatomía patológica
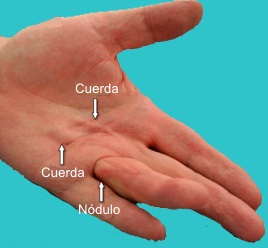
Desde el punto de vista macroscópico, en la enfermedad de Dupuytren se distinguen principalmente tres elementos: el nódulo, la cuerda y la contractura.
Los nódulos: Son bultos visibles o palpables en la base de los dedos, especialmente anular o meñique, aunque también pueden aparecer en el pulgar. Suelen ser el primer signo clínico y pueden preceder a la formación de cuerdas.
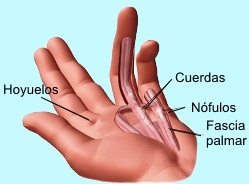
Las cuerdas: Son bandas fibrosas longitudinales que se extienden desde la palma hacia los dedos, generando contracturas en flexión al cruzar las articulaciones. Suelen acompañarse de nódulos, aunque también pueden aparecer de forma independiente. Cuando persisten, provocan rigidez articular y deformidades que dificultan las actividades diarias.
Los hoyuelos dérmicos: Son muescas profundas en la piel, a menudo localizadas en la palma o los dedos, causadas por la tracción de la piel hacia planos profundos debido a las cuerdas fibrosas. Pueden ser el primer signo o desarrollarse durante el curso de la enfermedad.
Acolchamientos articulares dorsales de Garrod: Son lesiones fibrosas situadas en el dorso de las articulaciones interfalángicas proximales, entre la piel y los ligamentos extensores.
Las cuerdas se derivan de las bandas normales de la aponeurosis palmar y pueden clasificarse según su origen:
- Cuerda pretendinosa: Proviene de bandas pretendinosas. Afecta a la articulación metacarpofalángica (MCF).
- Cuerda en espiral: Formada por la banda pretendinosa distal, banda espiral, lámina digital lateral y ligamento de Grayson. A medida que se engrosa, rodea y desplaza el paquete neurovascular hacia la línea media.

- Cuerda natatoria: Se origina en el ligamento natatorio y contribuye a contracturas del espacio palmar distal.
-
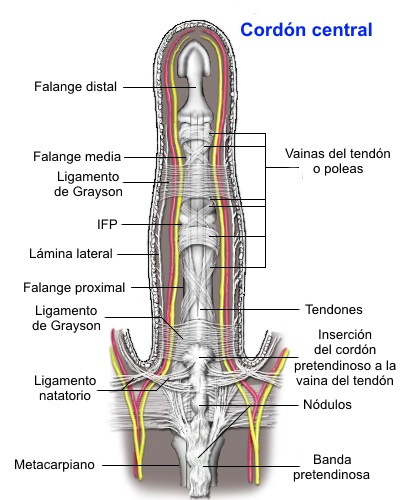
Cuerda central: Se localiza en la línea media del dedo, sin precursor fascial definido. Afecta principalmente la IFP, suele respetar los haces neurovasculares y puede unirse a la dermis.
-
- Cuerda lateral: Deriva de la banda digital lateral. Poco frecuente, se observa principalmente en el borde cubital del 5º dedo, en conexión con el abductor del 5º dedo.
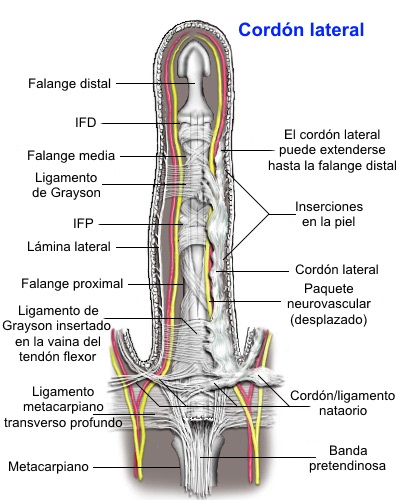
- Cuerda digital: Procede del tendón del abductor del 5º dedo. Atraviesa superficialmente el paquete neurovascular y puede insertarse en la falange media o distal.
- Cuerda retrovascular: Discurre profundamente al haz neurovascular, derivada de la banda retrovascular.
Estadios de la enfermedad de Dupuytren
La progresión de la enfermedad ocurre en tres fases:
- Fase proliferativa: Aparecen los nódulos con proliferación de miofibroblastos. Algunos pacientes refieren dolor o molestias por compresión nerviosa.
- Fase involutiva: Formación de cuerdas a lo largo de la fascia. Los miofibroblastos predominan y se alinean según líneas de tensión.
- Fase residual: La cuerda se tensa generando contractura. El nódulo desaparece, quedando colágeno acelular denso.
En esta fase final se invierte el patrón normal de colágeno: se incrementa el tipo III frente al tipo I.
Clasificación por gravedad:
- Grado 1: Nódulos y bandas en la aponeurosis palmar. Posibles alteraciones dérmicas.
- Grado 2: Cuerdas pretendinosas y digitales, con limitación de extensión.
- Grado 3: Contracturas en flexión establecidas.

Diátesis de Dupuytren
Término acuñado por Hueston, que define una forma más agresiva y recurrente de la enfermedad. Se caracteriza por:
- Inicio precoz
- Afectación bilateral
- Fuerte historia familiar
- Progresión rápida
- Alta tasa de recurrencia
Los pacientes pueden presentar fibromatosis ectópica: enfermedad de Ledderhose (plantar), enfermedad de Peyronie (peniana) o almohadillas de Garrod (nudillos).
Fisiopatología
El tejido patológico de Dupuytren presenta aumento de colágeno tipo III y predominancia de miofibroblastos. Estos actúan como célula efectora principal, con propiedades contráctiles y de síntesis extracelular.
A nivel molecular, mediadores como prostaglandina F2α y ácido lisofosfatídico incrementan la contracción, mientras que PGE1, PGE2 y bloqueadores del calcio la reducen. Factores de crecimiento (FGF, PDGF) aumentan la actividad fibroblástica.
Existe sobreexpresión del gen POSTN (periostina), implicado en la diferenciación y persistencia de miofibroblastos. Esta proteína también se observa en procesos de reparación tisular temprana.
El colágeno tipo III aumenta, y se altera el equilibrio entre colagenasas (MMPs) y sus inhibidores (TIMPs), lo que favorece la fibrosis. La contracción ocurre por transmisión de fuerzas desde los microfilamentos de actina al colágeno extracelular.
Etiología / Patogénesis
Se postula una base genética con eventos desencadenantes ambientales. La hipótesis más aceptada plantea que una persona genéticamente predispuesta sufre una lesión isquémica local (diabetes, tabaco, alcohol, trauma), que activa la vía de la xantina oxidasa. Esto genera radicales libres que estimulan la proliferación fibroblástica y la liberación de citocinas, especialmente IL-1 y TGF-β.
El LPA, producido por activación plaquetaria, promueve la contracción celular. La fibrosis también se relaciona con desequilibrio apoptótico y sobreexpresión de factores como MafB o POSTN. Se han identificado alteraciones genéticas (trisomía 7, 8) y mutaciones mitocondriales.
Otros factores etiológicos
- Edad avanzada
- Sexo masculino: 10 veces más frecuente
- Diabetes mellitus: Más común y grave en tipo 1
- Epilepsia: Posible relación con barbitúricos
- Hepatopatía alcohólica: Afecta hasta el 20%
- Tabaquismo: Riesgo triplicado
- Inmunogenética: Asociación con HLA-DRB1*15, DR3
- Trauma local
- Trabajo manual con vibración
- Hormonas androgénicas: Posible sensibilidad aumentada
- VIH: Asociación controvertida
Epidemiología
Frecuencia
Prevalencia del 4% al 39% en poblaciones del norte de Europa. También se documentan casos en Asia y África.
Raza
Predomina en caucásicos del norte europeo. Menos común en asiáticos, africanos e indígenas americanos.
Sexo
80% de los casos afectan a varones. Debuta antes en hombres y con mayor gravedad.
Mortalidad / Morbilidad
La enfermedad de Dupuytren no tiene impacto en la mortalidad. La morbilidad se relaciona con la limitación funcional progresiva y cambios en el estilo de vida.
Diagnóstico diferencial
Debe distinguirse de múltiples entidades:
- Tenosinovitis estenosante (dedo en gatillo)
- Ganglión
- Tumores de partes blandas (fibromas, lipomas, sarcomas)
- Quiropatía diabética
- Enfermedad articular (artritis reumatoide, tofos)
- Trastornos neurológicos (parálisis cubital)
- Cambios postraumáticos o cicatrices
- Otras fibromatosis (palmar, Peyronie, Ledderhose)
- Camptodactilia
- Hiperqueratosis
Historia clínica
Los síntomas iniciales suelen incluir disminución del rango de movimiento, pérdida de destreza y dificultad para introducir la mano en el bolsillo. Es importante indagar sobre factores de riesgo como alcoholismo, tabaquismo, epilepsia, diabetes, traumatismos, trabajos manuales con vibración y antecedentes familiares.
También debe evaluarse la existencia de cirugías previas y de otras localizaciones afectadas, como pies o pene. El paciente típico presenta engrosamiento indoloro o nódulos en la palma o dedos, con grados variables de contractura. El cuarto dedo es el más frecuentemente afectado, seguido del quinto. La afectación puede ser bilateral pero no suele ser simétrica, y la lateralidad no influye.
Los nódulos raramente son dolorosos, salvo si hay compresión nerviosa o tenosinovitis. Puede existir deformidad en flexión e imposibilidad para extender los dedos, pero sin alteraciones sensoriales salvo patología añadida. En fases avanzadas, la enfermedad suele ser indolora.
Examen físico
El diagnóstico suele ser clínico. Se deben explorar:
- Nódulos: Firmes, adheridos a piel, sensibles al tacto. Si se mueven con los tendones, no son característicos de Dupuytren.
- Cuerdas: Indoloras, situadas proximalmente a los nódulos.
- Alteraciones cutáneas: Palidez al extender dedos, surcos o depresiones por adherencias fasciales.
- Nódulos de Garrod: En el dorso de nudillos, presentes en 44–54% de los casos, sugieren evolución más agresiva.
- Fascia plantar (Ledderhose): Afectada en 6–31%, se asocia a mayor severidad.
- Contracturas articulares: A nivel de MCF e IFP, valorar ángulos y existencia de compensación o contractura en IFD.
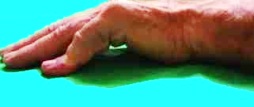
- Prueba de Hueston: Positiva si no se puede apoyar completamente la palma sobre una superficie plana. Se considera indicativa de cirugía si hay al menos 30° de contractura MCF.
Estudios de imagen
La resonancia magnética puede correlacionarse con los hallazgos intraoperatorios: las cuerdas son hipocelulares y los nódulos presentan mayor celularidad, lo que podría tener implicaciones pronósticas en cuanto a la recurrencia.
Educación del paciente
Se debe informar que la cirugía mejora la funcionalidad pero no cura la enfermedad. Es crucial explicar las posibles complicaciones, incluido el síndrome de dolor regional complejo. La rehabilitación intensa con terapeuta ocupacional es esencial para lograr un buen resultado funcional.
Tratamiento actual de la enfermedad de Dupuytren (Actualización 2024)
La enfermedad de Dupuytren es una fibromatosis benigna de la fascia palmar que provoca contracturas progresivas, especialmente en el anular y meñique. Aunque no tiene cura definitiva, los tratamientos actuales permiten mejorar la funcionalidad y controlar los síntomas.
1. Tratamiento no quirúrgico
A. Fármacos y terapias biológicas
Inyecciones de colagenasa Clostridium histolyticum (Xiaflex®): enzima que disuelve las cuerdas fibrosas. Se inyecta directamente y se realiza manipulación a las 24–48 h para romper la cuerda.
- Eficacia: 60–80 % de corrección en contracturas ≤ 50° (mejor en MCF que IFP).
- Ventajas: mínimamente invasivo, sin cicatriz.
- Limitaciones: recurrencia del 30–50 % a 5 años, hematomas, dolor postratamiento.
Corticoides intralesionales: útiles en nódulos dolorosos en fase inflamatoria inicial.
Terapias experimentales:
- Antifibróticos (5-fluorouracilo, inhibidores de TGF-β).
- Radioterapia superficial en fases muy iniciales (controvertida).
B. Fisioterapia y órtesis
- Movilización precoz tras tratamiento para evitar rigidez.
- Férulas nocturnas en extensión: utilidad limitada, recomendadas tras colagenasa o cirugía.
2. Tratamiento quirúrgico
A. Fasciotomía percutánea con aguja (PNA)
Indicada en cuerdas palpables sin afectación cutánea. Se realiza bajo anestesia local.
- Ventajas: recuperación rápida, bajo coste.
- Desventajas: recurrencia precoz (50–70 % a 3 años), riesgo de lesión nerviosa.
B. Fasciectomía limitada o selectiva
Indicada en contracturas > 30–40° en articulaciones MCF o IFP.
- Fasciectomía abierta: técnica de referencia en casos avanzados.
- Dermofasciectomía: en casos con afectación cutánea, se requiere injerto.
- Complicaciones: rigidez, hematomas, infección, lesión neurovascular.
C. Amputación
Opción extrema reservada para deformidades incapacitantes en recidivas múltiples.
3. Avances recientes
- Terapia génica: estudios con siRNA para inhibir genes profibróticos (TGF-β1, COL3A1).
- Lipofilling post-quirúrgico: reduce fibrosis y mejora vascularización.
- HIFU (ultrasonido focalizado de alta intensidad): en investigación como técnica no invasiva.
4. Manejo de recurrencias
El enfoque es escalonado: PNA → colagenasa → fasciectomía. La reintervención quirúrgica conlleva mayor riesgo por fibrosis y adherencias previas.
5. Factores pronósticos
| Factor | Riesgo de recurrencia |
|---|---|
| Edad < 50 años | Alto |
| Antecedentes familiares | Alto |
| Localización en IFP (vs MCF) | Mayor |
| Enfermedad bilateral | Alto |
Conclusión
El tratamiento debe adaptarse al grado de contractura (según la tabla de Tubiana), edad del paciente, demanda funcional, técnicas disponibles y riesgo de recurrencia. La tendencia actual es optar por procedimientos menos invasivos (colagenasa, PNA) y reservar la cirugía abierta para los casos complejos.
Tratamiento con Colagenasa (Xiaflex®) y Fasciotomía Percutánea con Aguja (PNA) en la Enfermedad de Dupuytren
Ambas técnicas son alternativas mínimamente invasivas a la cirugía abierta. Aunque persiguen el mismo objetivo (liberar la contractura), presentan diferencias importantes en mecanismo de acción, indicaciones, efectividad y perfil de complicaciones.
1. Colagenasa Clostridium histolyticum (Xiaflex®)
Mecanismo de acción
La enzima colagenasa degrada de forma selectiva el colágeno tipo I y III presente en las cuerdas fibrosas, debilitándolas y permitiendo su ruptura mediante extensión pasiva forzada.
Protocolo de aplicación
- Selección del paciente: contracturas ≥ 20° en MCF o ≥ 30° en IFP, cuerdas palpables bien definidas. No se recomienda en lesiones difusas, piel ulcerada, afectación neurovascular.
- Inyección: 0.58 mg por cuerda (máx. 2 por sesión). Inyección directa en la cuerda, no en el nódulo. Anestesia local opcional.
- Manipulación: a las 24–72 h se realiza extensión forzada del dedo bajo anestesia local para romper la cuerda.
Efectividad
- MCF: 70–80 % de corrección inicial (residuo ≤ 5°).
- IFP: 40–60 % de eficacia (menos efectiva por anatomía compleja).
- Recurrencia: 30–50 % a 5 años, más frecuente en IFP y en pacientes jóvenes.
Ventajas
- Tratamiento ambulatorio, sin cirugía.
- Recuperación rápida (1–2 días).
- Menor riesgo de rigidez o infección que cirugía convencional.
Efectos adversos
- Comunes: dolor local, edema, hematomas.
- Raros pero graves: rotura tendinosa, lesión neurovascular (0.1 %).
2. Fasciotomía percutánea con aguja (PNA)
Mecanismo
Consiste en cortar mecánicamente la cuerda mediante una aguja sin extraer tejido. No se emplea colagenasa ni se realiza incisión quirúrgica.
Protocolo
- Selección del paciente: cuerdas superficiales y aisladas, contracturas leves-moderadas, especialmente en MCF. Ideal en personas mayores con baja demanda funcional.
- Técnica: anestesia local con lidocaína sin epinefrina. Aguja hipodérmica (25G) utilizada con movimientos de vaivén para seccionar la cuerda. Idealmente guiada por ecografía.
- Postoperatorio: movilización inmediata; férula nocturna opcional para mantener extensión.
Efectividad
- MCF: 70–90 % de corrección inicial.
- IFP: aproximadamente 50 % de corrección.
- Recurrencia: 50–70 % a 3 años.
Ventajas
- Bajo coste (solo aguja y anestesia).
- No deja cicatriz y puede repetirse si recidiva.
- Menor dolor postoperatorio que la colagenasa.
Complicaciones
- Rotura cutánea (10 %).
- Lesión nerviosa (1–3 %).
- Ineficaz en cuerdas gruesas o profundas.
3. ¿Colagenasa o PNA? Comparación directa
| Parámetro | Colagenasa | PNA |
|---|---|---|
| Costo | Alto (≈ $1,500 por dosis) | Muy bajo (≈ $50) |
| Tiempo de recuperación | 1–2 días | Inmediato |
| Eficacia en MCF | 70–80 % | 70–90 % |
| Eficacia en IFP | 40–60 % | <50 % |
| Recurrencia | 30–50 % a 5 años | 50–70 % a 3 años |
| Complicaciones | Hematomas, dolor post-inyección | Lesión nerviosa, rotura cutánea |
4. Recomendaciones clínicas
- Primera opción en MCF: si hay acceso y presupuesto, preferir colagenasa (menor recurrencia).
- Alternativa en centros sin colagenasa: PNA es efectiva y viable.
- IFP: baja eficacia en ambas técnicas; considerar fasciectomía si hay contractura severa.
- Pacientes jóvenes: preferible colagenasa, ya que la recurrencia es más tardía.
- Recidivas: PNA puede repetirse sin problemas. La colagenasa es reutilizable hasta 2–3 veces por cuerda.
Conclusión
Colagenasa y PNA han transformado el abordaje de la enfermedad de Dupuytren, evitando muchas cirugías abiertas. Su elección depende de la localización, accesibilidad económica, tipo de cuerda y experiencia del profesional. La combinación de ambas estrategias permite optimizar resultados: colagenasa para cuerdas gruesas en MCF y PNA para lesiones finas o pacientes frágiles.
Conclusiones finales
La enfermedad de Dupuytren es una patología fibroproliferativa benigna, pero funcionalmente limitante, que afecta predominantemente a la fascia palmar de la mano. Su etiología multifactorial, evolución progresiva e impacto sobre la calidad de vida del paciente justifican la necesidad de una valoración individualizada y un abordaje terapéutico adaptado al grado de afectación funcional.
Si bien los tratamientos conservadores tienen un papel limitado, el abordaje quirúrgico sigue siendo el tratamiento de elección en los casos con contracturas significativas. Las distintas técnicas quirúrgicas, desde la fasciotomía hasta la fasciectomía radical y la dermofasciectomía, deben seleccionarse en función del estadio clínico, las comorbilidades del paciente y el riesgo de recidiva.
El seguimiento postoperatorio, la correcta inmovilización inicial y la rehabilitación funcional precoz son claves para optimizar los resultados clínicos y minimizar las complicaciones. A pesar del riesgo de recurrencia, el pronóstico global suele ser favorable, especialmente cuando la indicación quirúrgica y la ejecución técnica son adecuadas.
La comprensión profunda de los factores pronósticos, la experiencia quirúrgica y la colaboración multidisciplinar con fisioterapia especializada son fundamentales para ofrecer al paciente la mejor recuperación funcional posible.