Necrosis avascular cabeza femoral
Introducción y definición
La necrosis avascular es una enfermedad
debida a la pérdida temporal o permanente del flujo de sangre a los huesos. Esta
falta de flujo sanguíneo, en el caso de la cabeza femoral puede ser extraósea
cefálica (arterias retinaculares) en la necrosis postraumática, o por procesos
vasculares intracefálicos en las necrosis idiopáticas. Sea por una causa u otra,
el hueso trabecular se necrosa, conduciendo, a menudo al colapso de la
articulación. La necrosis avascular también se conoce como osteonecrosis,
necrosis isquémica, y necrosis aséptica, y afecta a hombres y mujeres de
cualquier edad, pero es más común entre los 30 y 40 años.
El desarrollo de la osteonecrosis puede
tener una repercusión importante sobre el estilo de vida del individuo. Puesto
que muchos de estos pacientes son jóvenes en el momento del diagnóstico, a
menudo deben introducir modificaciones en su trabajo y en sus actividades de
ocio. El objetivo final en el tratamiento de la osteonecrosis de la cadera es la
conservación de la cabeza femoral. Sin embargo, este objetivo resulta difícil de
lograr dado que la condición se asocia a diversas enfermedades y a que ni la
etiología ni la historia natural se han determinado de forma concluyente. El
diagnóstico de osteonecrosis supone de un 5 a un 12% de todas las artroplastias
de cadera.
Etiopatogenia y factores de riesgo
La necrosis isquémica de la cabeza femoral
es una entidad nosológica que abarca dos grandes grupos muy diferentes en su
etiopatogenia y evolutividad. (Glimcher y Kenzora en The biology
of osteonecrosis of human femoral head and its clinical implications. An abridget communication. Clin. Orthop., 130,
47, 1978).
- Necrosis postraumáticas avasculares.
- Necrosis idiopáticas, con el fin de no
prejuzgar el origen vascular de este segundo grupo, ya que su patogenia no
está aun claramente definida.
Básicamente, la diferencia entre ambos
grupos patogénicos se debe a una alteración macrovascular en las postraumáticas,
en contrapartida con la alteración de la microcirculación intracefálica de las
idiopáticas.
Dado que la osteonecrosis finalmente se
desarrolla en sólo un pequeño porcentaje de pacientes con cualquiera de estas
patologías, recientemente la atención se ha dirigido a comprender las
predisposiciones subyacentes al desarrollo de la osteonecrosis cuando concurren
factores ambientales. Actualmente el interés se centra en mutaciones genéticas
que conducen a una hipercoagulabilidad, la cual se traduce en microtrombosis y
osteonecrosis cuando actúan ciertos factores ambientales (epigenéticos). Los
pacientes que sufren la llamada osteonecrosis idiopática probablemente tienen
algún tipo de alteración de la coagulación que no se ha identificado.
Necrosis postraumática
El trauma es la causa más
común de necrosis avascular. Las necrosis avascular pueden ocurrir en el plazo
de 8 horas después de la interrupción traumática del flujo sanguíneo.
Necrosis post-fractura cervical
La causa de la isquemia es la interrupción
de los vasos retinaculares postero-superiores en una fractura desplazada del
cuello femoral. Una vez la cabeza ha quedado privada de su vascularización se va
isquemiando de forma progresiva, y no aguda, como sucede en los infartos.
La necrosis de la cabeza femoral puede
aparecer 10 años después de una fractura subcapital.
Las fracturas desplazadas del cuello femoral
se han asociado a una prevalencia de osteonecrosis del 15 al 50%, dependiendo
del tipo de fractura, tiempo transcurrido hasta su reducción y la exactitud de
ésta.
Necrosis post-luxación de cadera
Se ha publicado en distintas series que la
prevalencia de osteonecrosis tras una luxación de cadera es de un 10 a un 25%La
duración de la luxación puede que esté relacionada con el desarrollo final de
una osteonecrosis, siendo la prevalencia de osteonecrosis en luxaciones de más
de doce horas el doble que en luxaciones que se redujeron de urgencia.
Parece ser que la luxación posterior es la
más isquemizante, y que las luxaciones asociadas a fracturas incrementan la
probabilidad de necrosis isquémica.
Necrosis idiopática
Teorías
patogénicas
Factores intravasculares
- Factores arteriales extraóseos. Se cree que es el mecanismo más importante en el desarrollo de necrosis
avascular de la cabeza femoral. La cabeza femoral tiene un riesgo mayor de
desarrollar necrosis avascular, en parte porque el flujo de sangre es un
sistema órgano-termina con un desarrollo pobre de circulación colateral. El
traumatismo de la cadera puede conducir a una contusión o a una interrupción
mecánica de los vasos retinaculares laterales, que es la fuente principal de
sangre de la cabeza femoral y cuello. En un grupo grande de pacientes, la
arteriografía demostró arteritis estenosante y enfermedad arteriosclerosa de
los vasos retinaculares laterales, que puede ser una consideración
importante en los pacientes más viejos.
La vasculitis,
como se ha visto en la enfermedad de Raynaud, o el vasoespasmo, como se ha visto
en enfermedad de descompresión, puede interferir con la circulación extraósea.
La Interrupción extraósea de las arterias femorales circunflejas epifisarias
laterales y mediales se ha demostrado en necrosis avascular de la cabeza femoral
y en adultos jóvenes y en la enfermedad de Perthes por angiografía
súper-selectiva.
- Factores arteriales intraóseos. la etiología primaria aparece ser que ocurren microembolias en el interior
de los vasos que bloquean la microcirculación de la cabeza femoral. (Jones).
Existen varios factores que hacen a esta región especialmente sensible a las
microembolias, pues la necrosis ósea es muy rara en las zonas metáfiso-diafisarias,
siendo típica de las epífisis femoral y humeral: circulación terminal
crítica de Jones. El gradiente de presión intra medular desfavorable a la
epífisis y el pequeño calibre de los vasos subcondrales y su disposición
terminal son los principales responsables de este acumuló selectivo de
micro-émbolos. Los vasos sanguíneos se aproximan a la placa subcondral en
ángulo recto, se expanden en sinusoides y giran 180° sobre sí mismos antes
de formar el retorno venoso, estando encerrados en un estuche rígido
inextensible que hace difícil el desarrollo de colaterales.
Tales condiciones
pueden ocurrir en la anemia de células falciformes, enfermedad por descompresión
(fenómenos hiperbáricos), embolia grasa, fenómenos La obstrucción vascular de la
microcirculación se puede causar por los émbolos grasos, relacionado con la
hiperlipidemia asociada al alcoholismo, tratamiento con esteroides,
hiperuricemia, y burbujas de nitrógeno en la enfermedad de descompresión. Las vasculitis
también han sido propuestas como mecanismo de obstrucción vascular en esta
enfermedad, no solo como complicación de la terapia esteroidea sino como
afectación individualizada.
- Factores celulares citotóxicos. Relacionados con agresiones celulares directas, tales como las radiaciones
ionizantes.
- Factores venosos intraóseos. Las
anormalidades del retorno venoso en el interior de la cabeza femoral se ha
demostrado que favorece la necrosis avascular.
- Factores intraóseos extravasculares. El sistema
óseo dentro de la región subcondral de la cabeza femoral está incluido
dentro de una cáscara rígida de hueso cortical. Tal sistema es
particularmente sensible a los aumentos de presión dando por resultado un
síndrome compartimental. Ficat et al. Demostraron incrementos de presión en
la medular de los cuellos femorales en un gran número de pacientes con
necrosis avascular. Los primeros efectos de la presión elevada se dan en
los sinusoides y los pequeños capilares de la medular, además de en el
retorno venoso. Un espasmo reflejo el espasmo puede incluso bloquear los
arterias nutrientes antes de que entren en la corteza. Es la llamada teoría
compartimental, en la que los elementos que no pertenecen al árbol vascular
pueden, en condiciones patológicas. Comprimirlo extrínsecamente y reducir el
flujo circulatorio intramedular. Estos factores pueden afectar las células
grasas, elementos hematopoyéticos y reticuloendoteliales en el espacio
extravascular. Además de la población normal de la médula ósea existen otros
materiales celulares o inertes que se acumulan en el espacio intersticial de
la cabeza femoral, pudiendo causar una necrosis avascular.
- Factores capsulares. Se trata de enfermedades o procesos dentro de la articulación de la cadera
que producen efusiones, tales como traumatismos, infecciones, y artritis,
que pueden afectar negativamente al flujo de sangre a la epífisis. El
mecanismo implica el taponamiento de los vasos epifisarios laterales (la
fuente primaria de sangre a la epífisis), que están situadas dentro de
membrana sinovial, con una presión intracapsular creciente.
Procesos patógenos asociados a necrosis
avascular
Alcoholismo
El Alcohol puede tener efectos
tóxicos en las células osteogénicas. El efecto directo del alcohol resulta en
unos depósitos de grasa en el hígado. Los hígados grasos son fuente constante
de embolias grasas casi asintomáticas,
Las embolias grasas intraóseas
se hidrolizan a ácidos grasos libres, que dañan el endotelio vascular. La
ingesta de más de 40 ml de alcohol por semana incrementa el riesgo de necrosis
avascular más de 11 veces, comparado con el riesgo de los no bebedores. Existe
una clara relación de dosis respuesta.
Uso de
esteroides
Seis posibles mecanismos pueden estar
presentes
- Oclusión de pequeños vasos relacionados
con embolias grasas desde el hígado.
- Incremento de la presión intraósea
resultante de un incremento del tamaño de la gras intramedular relacionada
con esteroides, sin un perdida equivalente compensadora hueso trabecular y
cortical.
- Embolias grasas que se hidrolizan a
ácidos grasos libres, que son tóxicos para el endotelio vascular, provocando
una coagulación intravascular.
- Inhibición de la angiogénesis por una
reducción de actividad proteolítica para la síntesis de hormona antitiroidea
policlonal receptora de anticuerpos alfa-1.
- Un efecto tóxico directo sobre las
células osteogénicas.
- Los esteroides provocan una conversión
de la medula hematopoyética a medula grasa, que es un prerrequisito para
desarrollar una necrosis aséptica.
El riesgo es mayor en pacientes tratados con
altas dosis en corto espacio de tiempo, mas que una dosis acumulada o una
terapia prolongada a bajas dosis. En cuanto al riesgo con bajas dosis, hay
controversia. La necrosis puede aparecer hasta 3 años después del cese del
tratamiento. La necrosis causada por esteroides es mayor que la causada por
otros factores ya que subyace una desmineralización, y se ve incrementada la
osteolisis y favorecido el colapso.
Enfermedad por descompresión (barotraumatismos)
Se da en trabajadores que trabajan en
condiciones de hiperbarismo y que frecuentemente se ven sometidos a procesos de
descompresión.
Los factores de riesgo determinantes son la
profundidad, el número de inmersiones, la descompresión incontrolada,
concentraciones de oxígeno bajas, edad, obesos e hiperlipémicos. La presencia de
burbujas intravasculares de nitrógeno obstruyen los capilares.
Enfermedad metastásica
Las células metastásicas
pueden asentar en la medula resultando en un incremento de la presión
intramedular, obstruyendo los vasos intramedulares. Los pacientes tienen un
riesgo más elevado si reciben tratamiento con esteroides y/o reciben
radioterapia local en la cadera.
Pancreatitis
La liberación de encimas
pancreáticos en el torrente sanguíneo provoca la descomposición de la grasa de
las células medulares en ácidos grasos libres, que son tóxicos para el
endotelio, provocando una coagulación intravascular.
Hemoglobinopatías
falciformes
Las hemoglobinopatías son la
principal causa de necrosis avascular en países africanos. Los infartos en las
hemoglobinopatías son grandes. La necrosis avascular ocurre porque el fenómeno
de la drepanocitosis ocurre en los capilares y las vénulas, y provoca
hiperviscosidad y oclusión vascular.
Enfermedad de Gaucher
La enfermedad de Gaucher es
una enfermedad metabólica consistente en una deficiencia del encima
b-glucosidasa, que normalmente hidroliza el glucocerebrósido en glucosa y
ceramida. Con este defecto se produce un acúmulo de glucocerebrósidos en las
células reticuloendoteliales, provocando un aumento de la presión en la médula y
con ello de los sinusoides interóseos, provocando los infartos óseos.
Diálisis
Los niveles elevados de
parathormona incrementa el turn-over del hueso subcondral con reposición
desordenada de la matriz incapaz de soportar la carga normal, resultando en
microfracturas e incremento de la presión intramedular.
Radioterapia
La fibrosis y la proliferación
endotelial resultante de la radiación provocan una arteritis con compromiso
vascular, si además el paciente recibe quimioterapia y tratamiento con
esteroides el riesgo se incrementa. La necrosis avascular ocurre cuando se
superan los 30 Gy.
Hiperuricemia
La aparición de necrosis
avascular en estos pacientes viene determinada pos la asociación de varios
factores patogénicos: corticoterapia, etilismo asociado a obesidad y
sedentarismo con hiperlipemia, disfunción hepática, pancreatitis. En los casos
de hiperuricemia aislada se han demostrado cristales de uratos en el interior de
los vasos sanguíneos de las áreas perinecróticas.
Hemofilia
Las microhemorragias repetidas
en la medular ósea provocan un incremento de presión. La distensión capsular
provocada por una hemorragia también comprime los vasos retinaculares de la
capsula sinovial.
Estados de
hipercoagulabilidad
Deficiencias en proteínas
específicas inhibidoras de la cascada de coagulación, desordenes en el sistema
fibrinolítico. La hiperfibrinogenemia provoca un estado de hipercoagulablidad y
se asocia con un aumento de la agregación de los eritrocitos y una
hiperviscosidad, resultando en una disminución del flujo sanguíneo y en una
isquemia.
La hiperfibrinogenemia se ha
visto en pacientes con hiperlipoproteinemia (tipos II y IV), pacientes
fumadores, diabéticos, y con el uso de contraceptivos.
Estados de hipercoagulabilidad adquirida
Cuando se superponen factores
hereditarios subyacentes y factores adquiridos se incrementa el riesgo de una
trombosis vascular.
- La enfermedad de
Legg-Calvé-Perthes es la causa más frecuente de necrosis avascular en
niños.
- Deslizamiento de la
epífisis proximal del fémur.
- Luxación congénita de
cadera.
- Hígado graso.
- Fractura del cuello
femoral.
- Anemia de células
falciformes.
- Embarazo.
Clasificación
Clasificaciones
radiológicas de la osteonecrosis de la cabeza femoral
|
Sistema de
clasificación de Arlet y Ficat |
|
Estadio
|
Línea articular
|
Contorno de la cabeza
|
Trabeculado
|
Diagnóstico por Rx
|
Diagnóstico por exploración ósea
|
|
I
|
Normal |
Normal |
Normal uosteoporó-tico
|
Imposible |
Probable por pruebas
hemodiná-micas |
|
II
|
Normal |
Normal |
Osteoporosis o
esclerosis |
Probable |
Histopatogenia certera |
|
III
|
Normal |
Aplanamiento (colapso
del hueso subcondral) |
Formación de secuestro
|
Certero |
Confirmada |
|
IV
|
Estrechamiento |
Colapso |
Destrucción del polo
superior |
Muy difícil de
diferenciar entre osteoartrosis y osteonecrosis |
Insuficiencia
hemodinámica con necesidad de biopsia |
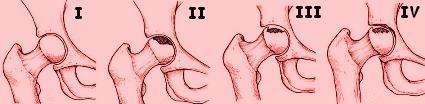
Clasificación
radiológica de Ficat y Arlet
|
Sistema de
clasificación y estadiaje
de la Universidad de Pensilvania |
|
Estadío 0 |
Normal o Rx,
gammagrafía o RMN no diagnósticas |
|
Estadío I |
Radiografía
normal con RMN o gammagrafía alteradas |
|
A |
Ligero
(alteración de la cabeza <15%) |
|
B |
Moderado (15
al 30% de cabeza afectada) |
|
C |
Severo (más
del 30% de la cabeza afectada) |
|
Estadío II |
Cambios de
lucencia y esclerosis en la cabeza femoral |
|
A |
Ligeros
(alteración de la cabeza <15%) |
|
B |
Moderados
(15 al 30% de cabeza afectada |
|
C |
Severos (más
del 30% de la cabeza afectada) |
|
Estadío III |
Colapso
subcondral (media luna) sin aplanamiento |
|
A |
Ligero (>15%
de la superficie articular) |
|
B |
Moderado
(15-30% de la superficie articular) |
|
C |
Severo (>30%
de la superficie articular) |
|
Estadío IV |
Aplanamiento
de la cabeza femoral |
|
A |
Ligero (<15%
de la superficie y depresión <2mm) |
|
B |
Moderado
(15-30% de la superficie o 2-4 mm. de depresión) |
|
C |
Severo (>30%
de la superficie o >4mm de depresión) |
|
Estadío V |
Estrechamiento de la interlínea y/o cambios acetabulares |
|
A |
Discretos |
|
B |
Moderados |
|
C |
Severos |
|
Estadío VI |
Cambios
degenerativos avanzados |
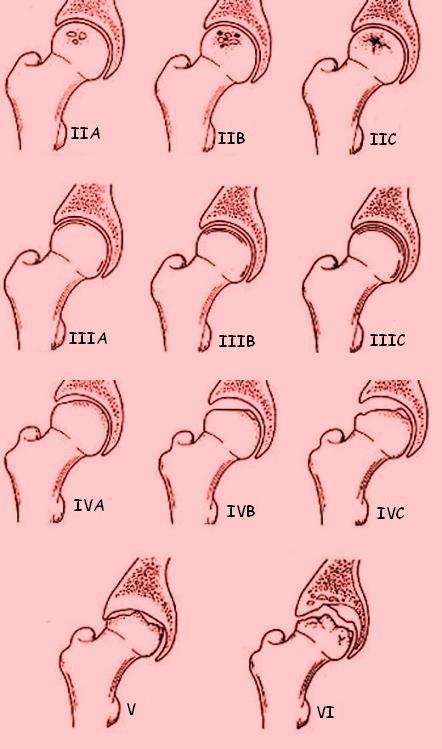
Clasificación
radiológica de la Universidad de Pensilvania
Tratamiento
El tratamiento específico de cada caso debe
estar en función del momento evolutivo del proceso, extensión de la isquemia o
sea, edad del enfermo y conocimiento previo del patobiología referida a la
función de la cabeza femoral. Además de estos factores de orden local cabe
destacar que la elección del tratamiento de cada paciente dependerá también del
nivel de actividad habitual, sintomatología y limitaciones funcionales,
colaboración ante el tratamiento, aceptación bilateral.
Por otra parte, la elección terapéutica
deberá hacerse en virtud del estadio radiológico, aunque no es infrecuente
encontrar caderas que presentan una destrucción radiológica prácticamente total,
pero que, sin embargo, son bien tolerada funcionalmente.
La tendencia actual en el tratamiento de la
necrosis isquémica de la cabeza femoral es la conservación de la cabeza femoral
en aquellos casos en que las lesiones no sean muy evolutivas (estadios
iniciales). Esta idea se debe fundamentalmente al hecho de que los enfermos
afectos de necrosis isquémica de la cabeza femoral tienen una edad considerada
como de "preremplazamiento articular" por ello no parece lógica la sustitución
parcial o total de la cadera por prótesis artificiales, excepto en aquellos
casos evolucionados o invalidantes.
Tratamiento no quirúrgico
El tratamiento no quirúrgico
generalmente tiene un pronóstico pobre. La marcha en descarga se asocia a un
índice mayor del 85% de colapso de la cabeza femoral. Según Mont y Hungerford
solo se salvaron el 35% de las cabezas femorales en estadío I, el 31% en estadío
II y solo el 13% en estadio III. Sin embargo la descarga puede ser eficaz en
lesiones localizadas en la porción intermedia de la cabeza femoral.
Tratamiento Quirúrgico
Descompresión del núcleo
La descompresión de la cabeza es el procedimiento
utilizado con más frecuencia en el tratamiento de los estadíos precoces de la
osteonecrosis de la cabeza femoral. Sin embargo, aunque este procedimiento se ha
empleado durante aproximadamente tres décadas y existen numerosos trabajos que
analizan su eficacia, no hay un consenso general en cuanto a las indicaciones de
este procedimiento o las técnicas que optimizan sus resultados. Mont y
Hungerford divulgaron un índice de éxitos de el 84% y el 65% para la enfermedad
en el estadío I y en estadío II, respectivamente. La descompresión de la médula
es más eficaz cuando menos el de 30% de la cabeza femoral está afectada. No
obstante, a pesar de los numerosos estudios, la verdadera tasa de éxitos de la
descompresión del núcleo es difícil de determinar por las diferencias entre los
diversos estudios en cuanto a selección de pacientes (ej. diferencias en los
diagnósticos), sistemas de clasificación, procedimientos quirúrgicos,
tratamiento postoperatorio y valoración del resultado clínico.
Steinverg evaluó retrospectivamente 297 caderas en 205
pacientes sometidos a descompresión del núcleo combinada con la colocación de
injerto esponjoso en el trayecto de la descompresión y que habían sido seguidos
durante un mínimo de dos años. Este autor concluyó que el estadío y localización
de la lesión influyen claramente sobre los resultados de la técnica. Se precisó
artroplastia total de cadera en un 22% de las caderas en estadíos I y II con un
área afectada pequeña (estadíos IA y IIA). En comparación, 39% de las caderas en
estadío I y el 40% de las caderas en estadío II con afectación del 15% de la
cabeza (estadíos IB, IIB y IIC) requirieron finalmente una artroplastia total.
Injertos osteomusculares
Los resultados obtenidos con este método en
el tratamiento de la necrosis isquémica de la cabeza femoral establecida, sobre
todo la no traumática, no son tan esperanzadores como los preventivos de la
necrosis isquémica de la cabeza femoral post-fractura cervical. Aunque
ideológicamente el método es adecuado, el injerto pediculado no proporciona
suficiente vascularización al foco isquémico, ni posee capacidad osteogénica
como para prevenir las secuelas secundarias tardías (colapso segmentario,
coxartrosis...).
Injerto óseo no vascularizado
Esta técnica fue descrita por Phemister. La filosofía de la misma, en mi idea de los autores,
que era el " drilling " de la cabeza femoral, no sólo para escindir el tejido
necrótico, sino también para permitir la rápida inversión y transformación
basculan de la cabeza femoral. Los tallos óseos corticales darían estabilidad a
la fractura cervical, favoreciendo la revascularización y previniendo el colapso
segmentario cefálico.
En los últimos años, la técnica de Phemister ha sido
abandonada por la mayoría de los autores a tenor de los irregulares resultados
obtenidos con ella. Hay que significar que el beneficio que proporciona este
procedimiento es exclusivo de aquellos casos muy precoces, unilaterales y no
esteroideo, y sólo cuando el injerto es colocado correctamente.
Injertos libres vascularizados de peroné
La utilización de injertos óseos
vascularizados para tratar la osteonecrosis de la cabeza femoral se inició para
prevenir el colapso de la cabeza y para estimular la vascularización del hueso
en esta región.
El principio de estas intervenciones es la eliminación de
la totalidad de hueso necrótico y su emplazamiento por un injerto, córtico-esponjoso
vascularizados al cual se asociarían chips de esponjosa. Con este procedimiento
cabe esperar una revascularización completa del foco necrótico a partir del
injerto y sus vasos, que, además, aportan, células osteoprogenitoras.
La transferencia de un injerto óseo vascularizados permite
la conservación de su patrón vascular intrínseco la conservación de la
circulación periostal y medular del incierto permite asegurar mantenimiento y
viabilidad del área perivascular y perisinusoidal. En estas circunstancias, la
BMP de la cortical y medular del injerto libre vascularizado pueden actuar
sobre una amplia población de "células diana", las cuales, bajo su influencia,
se transformarán en células productoras de nuevo hueso.
También cabe indicar que la capacidad de expansión
neovascular de los injertos libres vascularizados que permitirá la aparición de
nuevas generaciones de células pluripotenciales capaces de ser moduladas por la
BMP.
Basados en este razonamiento, los injertos libres
vascularizados tienen todos los condicionamientos necesarios para inducir la
osteogénesis y la reparación de un hueso y isquémico: 1) estructuras vasculares
y perivasculares, con el consiguiente aporte de células osteogénicas y
precursoras (pericitos, células mesenquimales, endoteliales,
retículo-monocitoides...), y 2) estructuras óseas, cortical y medular en donde
se encuentran concentraciones elevadas de proteínas morfogenética ósea capaz de
actuar sobre las células precursoras y derivarlas en osteoblastos, que serán, en
definitiva, las células que reparen el hueso necrótico.
Aunque los injertos de peroné vascularizados han
demostrado su éxito, existen algunas desventajas potenciales de esta compleja
técnica quirúrgica. En primer lugar, las complicaciones asociadas con la
obtención del peroné. En una revisión de 198 pacientes (247 injertos de peroné
libre vascularizado), Vail y Urbaniak publicaron una tasa de complicaciones del
19%, incluyendo debilidad motora, molestias subjetivas en el tobillo y otros
lugares de la extremidad y anomalías sensitivas en el miembro inferior. La
prevalencia de dolor en el tobillo y en la extremidad se incrementó con el
tiempo y era de un 11.5% a los cinco años de la intervención. Además, la tasa de
fracturas del fémur proximal después de utilizar un injerto de peroné fue de un
2.5% (dieciocho de 707) en una gran serie.
Las indicaciones relativas de la técnica en pacientes con
osteonecrosis continúan evolucionando. En este momento, generalmente se reserva
a los pacientes sintomáticos. Es una opción razonable en pacientes menores de
cincuenta años sin colapso de la cabeza femoral. La técnica es más controvertida
en pacientes con colapso de la cabeza femoral y su utilización debe decidirse en
base al diagnóstico, la edad del paciente y la progresión de la enfermedad.
Deben considerarse otras opciones de tratamiento en pacientes mayores de
cuarenta años con una afectación extensa de la cabeza femoral y evidencia de
colapso.
Osteotomías
El fundamento de una osteotomía se basa en el efecto
biomecánica de retirar el segmento necrótico o colapsado de la cabeza femoral
del área principal de carga de la cadera. Algunos
autores han atribuido la eficacia de las osteotomías a la reducción de la
hipertensión venosa y la disminución consiguiente de la presión intramedular que
se producen después de estos procedimientos. Las osteotomías no son ampliamente aceptadas como un
método estándar en el tratamiento de la osteonecrosis de la cabeza femoral
porque sus resultados han sido variables y por la dificultad de convertir los
casos fracasados en prótesis de cadera.
Artroplastia femoral de revestimiento
limitada (de resuperficialización)
La artroplastia o hemiartroplastia femoral de
revestimiento limitada es una opción viable en pacientes jóvenes que tienen una
lesión extensa precolapso o una lesión postcolapso sin afectación acetabular. Esta artroplastia se basa en la idea del
reparto de presiones sobre la cabeza femoral, favoreciendo secundariamente la
rehabilitación del secuestro y la colocación de una superficie de carga
homog6nea que no deteriore el cotilo sano. Igualmente, el mantenimiento del
muñón femoral diferirá la artroplastia total de la cadera y la facilitara en el
caso de necesitarse. Este procedimiento cuenta con algunas ventajas: (1) se extirpa el cartílago
dañado de la cabeza femoral, (2) preserva la reserva
ósea de la cabeza y cuello femorales y (3) la revisión a una
artroplastia total subsiguiente no se complica. Cuando hay una afectación de la cabeza femoral de
moderada a severa, una artroplastia total de cadera puede ser la única
alternativa. Puesto que la osteonecrosis es una enfermedad que frecuentemente
afecta a pacientes en la tercera, cuarta o quinta décadas de la vida (media de
edad de treinta y seis años), si el revestimiento de la cabeza femoral puede
retrasar la necesidad de una artroplastia total de forma predecible, se
convierte en una opción viable. Se requieren más estudios para determinar las
indicaciones específicas del revestimiento de la cabeza femoral. Existe un
acuerdo general en que va mejor si se realiza antes de que se haya producido una
degeneración sustancial del cartílago acetabular. Los candidatos potenciales
para un revestimiento limitado de la cabeza femoral son (1) pacientes jóvenes
con degeneración mínima o ausente del cartílago acetabular que se presentan con
un signo de la media luna o con colapso de la cabeza femoral y (2) pacientes
jóvenes sin colapso de la cabeza pero con afectación osteonecrótica extensa de
la misma (un ángulo de necrosis combinado mayor de 200º o una afectación de la
cabeza superior al 50%). Sin embargo, el paciente debe ser advertido de que el
grado de alivio del dolor que sigue a un procedimiento de recubrimiento de la
cabeza no es tan consistente como el que se logra con una artroplastia total y
los pacientes de cincuenta años de edad o mayores pueden tener mejor resultado
con una artroplastia total de cadera.
Prótesis totales
Los avances conseguidos en los últimos años en el
conocimiento de la bioincorporación de los materiales al organismo ha hecho
posible la mejora de los diseños v de los resultados de las artroplastias
totales de cadera. De las múltiples
intervenciones disponibles para tratar la osteonecrosis de la cabeza femoral, la
artroplastia total es el tratamiento con mayor probabilidad de conseguir un
alivio precoz y excelente del dolor y un buen resultado funcional. Estas
ventajas de la artroplastia total deben sopesarse frente al hecho de que
sacrifica más hueso y limita futuras opciones de tratamiento más que otros
procedimientos. Las principales
indicaciones de la artroplastia total son (1) osteonecrosis de la
cabeza femoral con cambios degenerativos secundarios avanzados con lesión severa
del cartílago articular de la cabeza y pérdida del cartílago acetabular y (2) un paciente mayor o con
bajas demandas funcionales con afectación extensa o colapso de la cabeza femoral
que tiene síntomas suficientes para justificar una artroplastia total de cadera. En estos dos grupos de pacientes, la artroplastia total es el método más fiable
para aliviar el dolor y recuperar la función precozmente con una sola
intervención. Los grupos principales en que está contraindicada la artroplastia total son (1) pacientes jóvenes con
una osteonecrosis de la cabeza femoral en estadío precoz en que son viables
otras opciones de tratamiento que conservan la cabeza y (2) pacientes con un riesgo
excesivo de complicaciones con una artroplastia total (por ejemplo, aquellos con
un hábito alcohólico grave y permanente que tendrían un riesgo excesivo de
luxación de una prótesis total). Un número relativamente alto de pacientes, especialmente aquellos de edad media
con un grado variable de afectación de la cabeza y colapso, caen dentro de una
zona gris en la cual la artroplastia total es una entre varias opciones de
tratamiento, incluyendo la hemiartroplastia de revestimiento. La artroplastia total de cadera ha producido de manera predecible un alivio
excelente del dolor y una mejora funcional en pacientes con osteonecrosis de la
cabeza femoral
References
1. Hungerford DS, Zizic TM: Pathogenesis of ischemic necrosis of the femoral
head. Hip 249-262, 1983.
2. Hopson CN, Siverhus SW: Ischemic necrosis of the femoral head: treatment by
core decompression. J Bone Joint Surg [Am] 70A:1048-1051, 1988.
3. Mitchell DG, Rao VM, Dalinka MK, et al.: Femoral head avascular necrosis:
correlation of MR imaging, radiographic staging, radionuclide imaging, and
clinical findings. Radiology 162:709-15, 1987.
4. Turner DA, Templeton AC, Selzer PM, Rosenberg AG, Petasnick JP: Femoral
capital osteonecrosis: MR finding of diffuse marrow abnormalities without focal
lesions. Radiology 171:135-40, 1989.
5. Ficat RP, Arlet J. Necrosis of the femoral head. In: D. S. Hungerford, ed.
Ischemia and necross of bone. Baltimore: Williams and Wilkins, 1980: 171-182.
6. Lafforgue P, Dahan E, Chagnaud C, Schiano A, Kasbarian M, Acquaviva PC:
Early-stage avascular necrosis of the femoral head: MR imaging for prognosis in
31 cases with at least 2 years of follow-up. Radiology 187:199-204, 1993.
7. Bluemke DA, Petri M, Zerhouni EA: Femoral head perfusion and composition: MRI
and MRS evaluation in patients at risk for avascular necrosis. Radiology
197:433-438, 1995.
8. Hayes CW, Conway WF, Daniel WW: MR imaging of bone marrow edema pattern:
transient osteoporosis, transient bone marrow edema syndrome or osteonecrosis. Radiographics
13:1001-1011, 1993.
|