|
Lesiones condrales-Osteocondrales
Los defectos condrales u osteocondrales generados
en el cartílago articular, agudos o crónicos, como resultado de
fuerzas excesivas de compresión en el espesor del tejido
cartilaginoso o de cizallamiento a nivel subcondral, tienden a
evolucionar, con el tiempo, hacía procesos degenerativos que, en las
personas de más edad son, normalmente tratados mediante la
sustitución total de la articulación por una prótesis artificial,
pero que en pacientes jóvenes, por el contrario, este tipo de
defectos deben ser solucionados antes de que se generen patologías
más severas.
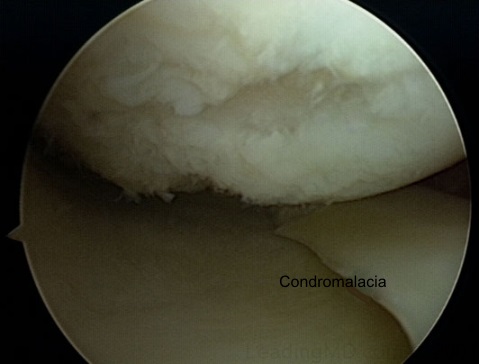
Las lesiones osteocondrales
representan una entidad diferente a las condrales y en bastantes
ocasiones se asocia a una lesión de los ligamentos. Por definición
abarcan el cartílago articular y el hueso subcondral adyacente.
Etiología
La etiología y fisiopatología de
estas lesiones es multifactorial. Dentro de las más frecuentes se
encuentra los traumatismos directos o por torsión y la
osteocondritis disecante. Aunque a esta última se le adjudican
múltiples causas, en general el tratamiento se basa en los mismos
principios de manejo de las fracturas osteocondrales.
Pueden producirse tres grados de
lesiones titulares:
-
Alteraciones de las células y
matriz extracelular sin lesión macroscópica de la superficie
articular.
-
Lesión macroscópica del cartílago
articular sin afectación del hueso subcondral.
-
Lesión macroscópica del cartílago
articular y el hueso subcondral subyacente. Es la fractura
osteocondral.
Las lesiones microscópicas del
cartílago articular pueden ser debidas a un traumatismo único o a
microtraumatismos repetidos. Independiente de la causa se observan
bandas de condrocitos muertos que dificultan los procesos de
degradación y síntesis de la matriz extracelular, como consecuencia
hay una disminución de proteoglicanos y una desorganización
ultraestructural del colágeno y aumento de la hidratación tisular.
Estos cambios provocan un aumento de la permeabilidad y una
disminución de su rigidez.
Las lesiones condrales abarcan
la capa cartilaginosa más blanda y suelen localizarse en el cóndilo
femoral lateral y la superficie medial de la rótula. Estas lesiones
se encuentran en personas con esqueleto maduro, a diferencia de las
fracturas osteocondrales que suelen afectar a pacientes con
esqueleto inmaduro. En este caso los traumatismos son de mayor
energía que en las lesiones microscópicas del cartílago articular.
La mayoría de los defectos condrales están asociados con daño a
otros tejidos de la rodilla.
En las zonas en que se ha producido
el impacto se aprecian lesiones macroscópicas del cartílago que
pueden consistir en fisuras o fragmentos desprendidos pero que no
afectan al hueso subcondral. La producción de estas lesiones no
ocasiona hemorragia intraarticular ni respuesta inflamatoria, ya que
el tejido cartilaginoso es avascular.
Los condrocitos responden
sintetizando matriz, pero en cantidad insuficiente para reparar todo
el defecto.
La lesión del cartílago articular, puede asociarse a procesos
degenerativos y de tipo traumático, que pueden ser agudos o
crónicos.
Manifestaciones clínicas:
-
Dolor.
-
Crepitación.
-
Bloqueos si existen fragmentos
desprendidos.
-
Puede haber derrame articular por
irritación de la sinovial.
-
El diagnóstico se basa en la
clínica y en al resonancia magnética y se confirma con una
artroscopia.
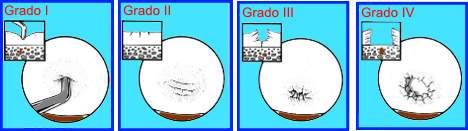
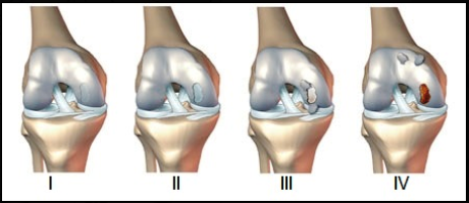
La clasificación más usada para
describir las lesiones condrales es la propuesta por Outerbridge, la
cual divide las lesiones en cuatro grupos:
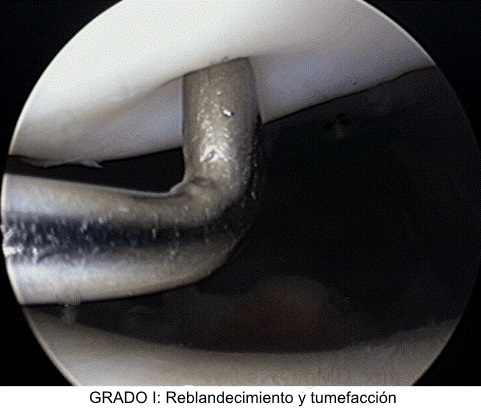
Grado 1. Reblandecimiento y
tumefacción del cartílago articular en un área irregular.
Grado 2. Existe fragmentación
y fisuración
Grado 3. La fragmentación y
fisuración se extienden hasta el área del hueso subcondral.
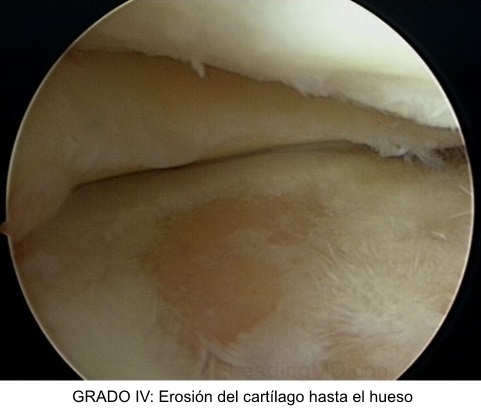
Grado 4. Se observa el hueso
subcondral expuesto.

| CClasificación
de las lesiones condrales |
| Grado |
Outerbridge |
ICRS |
|
0 |
Cartílago intacto |
Cartílago intacto |
|
1 |
Reblandecimiento y
tumefacción del cartílago articular en un área irregular |
Superficial (indentación
suave o fisuras |
|
2 |
Defecto de espesor parcial
con fisuras en la superficie que no alcanzan el hueso
subcondral o exceden 1,5 cm de diámetro |
Lesión menor de 50% del
grosor del cartílago |
|
3 |
Fisuración al nivel del
hueso subcondral en una zona con un diámetro de más de 1,5
cm |
Lesión mayor de 50% del grosor del cartílago |
|
4 |
Hueso subcondral expuesto |
Lesión que se extiende
hasta el hueso subcondral |
|
ICRS: International
Cartilage Repair |
En la fractura osteocondral, a
diferencia de aquella limitada al cartílago, la lesión incluye
cartílago y hueso subcondral, y se evidencia hemorragia y formación
de coágulo de fibrina que activa la respuesta inflamatoria alterando
el líquido sinovial. La reacción inflamatoria y el coágulo de
fibrina se extienden sobre la superficie articular dependiente de la
lesión, las plaquetas que participan de esta reacción liberan
factores mediadores vasoactivos y factores de crecimiento o
citoquinas que son proteínas que influencian múltiples funciones
celulares.
Dado que también hay compromiso óseo,
la matriz extracelular a este nivel también participa, con múltiples
factores de crecimiento que contribuyen de manera importante en la
curación, estimulando la invasión vascular y la migración de células
indiferenciadas que evolucionarán a condrocitos con todas sus
capacidades funcionales.
En la parte ósea de la lesión se
genera tejido óseo inmaduro que posteriormente se transformará en
maduro. Al final se produce un tejido cartilaginoso estructuralmente
similar al normal, pero que con el paso del tiempo va perdiendo
condrocitos y proteoglicanos y la matriz extracelular acaba
consistiendo en colágeno tipo I. Posteriormente a lo largo del
primer año, este tejido se desintegra y deja zonas expuestas de
hueso subcondral.
Diagnóstico
En ocasiones el diagnóstico es
difícil debido a que la historia y los síntomas imitan a la lesión
meniscal y en muchos casos pasa inadvertida.
El mecanismo lesional es variable:
impacto directo, avulsión, fuerzas torsión, fuerzas de
cizallamiento, etcétera.
Hay que buscar puntos dolorosos
electivos y sobre todo la presencia de un hidrartros con gotas de
grasa, que es patognomónico de una fractura osteocondral; la
fractura condral puede producir liquido amarillento. Pensaremos en
esta patología ante una clínica de evolución tórpida y con síntomas
aparentemente desproporcionados y persistentes y con imágenes
radiografías poco aparentes. Debemos buscar pequeños fragmentos en
las radiografías. De gran utilidad es la RM y finalmente la
artroscopia, que puede ser en determinados casos, terapéutica.
Tratamiento
La imposibilidad del cartílago
hialino para reparar sus propias lesiones hace que el tratamiento de
las pérdidas focales del cartílago articular sea un tema que este en
constante debate y cuyo tratamiento no esté resuelto por el momento.
Existen opiniones muy variadas
respecto al tratamiento de los casos asintomáticos. La evolución
natural de estas lesiones es desconocida. No existe ningún estudio
comparativo de los resultados del tratamiento quirúrgico y no
quirúrgico.
Las lesiones del cartílago articular
se dividen en:
La artroscopia es el mejor método
para corroborar el diagnóstico, localización y tipo de lesión.
Además nos permite instaurar un tratamiento quirúrgico a la vez.
Es importante reseñar que muchas de
estas lesiones se producen por que los pacientes tienen alteraciones
mecánicas, que conviene corregir para facilitar la reparación del
cartílago articular, por ejemplo las desviaciones en varo excesivo,
las insuficiencias ligamentosas o lesiones meniscales.
Se han propuesto diversas técnicas
quirúrgicas para tratar los defectos condrales, que incluyen,
técnicas de reparación, como lavado artroscópico o estimulación del
hueso subcondral y técnicas de regeneración como aloinjertos
osteocondrales , injerto osteocondral autólogo (mosaicoplastia),
implantación de condrocitos autólogo cultivados (ICA) y el implante
de fibras de carbón.
Las lesiones agudas sin
desplazamiento se pueden tratar con medidas conservadoras, sobre
todo inmovilización. Las lesiones crónicas pueden dejarse
evolucionar a menos que se identifique un fragmento suelto. En tal
caso se puede proceder a la eliminación quirúrgica del mismo.
Hay que reponer los fragmentos
grandes, sobre todo en zonas de carga y fijarlos.
Extraer los fragmentos pequeños
situados en zonas marginales. En el caso de lesiones cartilaginosas
localizadas que llegan al hueso subcondral pueden plantearse las
perforaciones tipo Pridie o la artroplastia artroscópica con
abrasiones superficiales, con resultados dispares.
Se están empleando últimamente discos
de fibras de carbono introducidos en los defectos osteocondrales,
esperando que se produzca una formación de colagenasa y una reacción
fibrosa que cubra el defecto. Se desconoce el resultado a largo
plazo también se han iniciado el recubrimiento de los defectos
condrales con injertos de pericondrio y periostio. También faltan
resultados a largo plazo.
En las fracturas osteocondrales y en la osteocondritis, la reducción
debe ser anatómica y la fijación debe ser estable para lograr una
curación de los tejidos y preferiblemente lo más pronto posible para
evitar la remodelación del fragmento.
Las lesiones en las que se utiliza
los métodos de fijación son aquéllas in situ que presentan:
desprendimiento o inestabilidad, persistencia de sintomatología,
actividad gammagráfica persistente o progresiva y por otro lado
aquéllas lesiones desplazadas que sean susceptibles de fijación, es
decir, aquellas que no son muy pequeñas, multifragmentarias, sin
adecuada superficie de contacto o que sean masivas.
Dentro de las posibilidades que se
tienen para la fijación están: las suturas, las sustancias
biodegradables (clavos ácido politáctico, polidioxaona, fibras de
carbono), sustancias adhesivas (sellantes de fibrina, pegantes
tisulares, adhesivos de cianoacrilato, polimetilmetacrilato), clavos
lisos, tornillos, tornillos canulados o de Herbert, y los clavos
óseos. Estos últimos son ampliamente utilizados, ya que presentan
entre sus ventajas la integración más sencilla y rápida del
fragmento, sin requerir una segunda intervención para la extracción
de los mismos, proporcionando una fijación estable que permite una
rehabilitación precoz del paciente.
La curación se hace de manera
secuencial evidenciándose puentes trabeculares óseos inmaduros a la
segunda semana y trabéculas maduras en la sexta semana. Los
fragmentos sueltos o no integrados se verán amarillos, descoloridos,
opacos, con abundante depósito de fibrocartílago tanto del defecto
como en la superficie de contacto y con evidencia temprana de
necrosis. En todos los casos la sinovial se observará con reacción
inflamatoria crónica e hipercelularidad.
En los casos en que no se pueda usar
la reducción y fijación del fragmento se dispone de las siguientes
técnicas:
Estimular la autoreparación
condral por parte del organismo:
Desbridamiento. Permite eliminar fragmentos de
cartílago y meniscos, con lo que mejora la función articular si bien
la duración de esta mejoría esta limitada en el tiempo. Quizá se
consiga lo mismo con un lavado articular.
Abrasión
y perforaciones. Esto pretende estimular el hueso
subcondral para que produzca fibrocartílago y cartílago hialino. Con
la abrasión del extremo óseo se penetra de 1-3 mm. de profundidad y
destruye vasos y cortical, llegando a hueso subcondral. Mientras que
con las perforaciones el agujero practicado se rellenará de tejido
fibroso o fibrocartílago, pero nunca de cartílago hialino. Los
resultados son impredecibles. Parte de la mejoría que experimentan
estos pacientes se debe a la limpieza de los fragmentos del
cartílago inestables, a la limpieza de cuerpos sueltos y a la
extracción de líquido sinovial.
Injerto
de pericondrio, hecho experimental KON (1981), tiene
algunas importantes interrogantes, la duración del injerto, el
riesgo de calcificación, etc... No parece tener buenos resultados.
Injertos
periósticos. Se basa en que en la capa profunda del
periostio hay células mesenquimales pluripotenciales. Con esta
técnica se intenta cubrir el defecto con una lámina de periostio de
manera que las células pluripotenciales se diferencien en sentido
condral y produzcan un tejido similar al cartílago hialino
articular. Los resultados son variables, pero parecen ser mejores en
personas jóvenes.
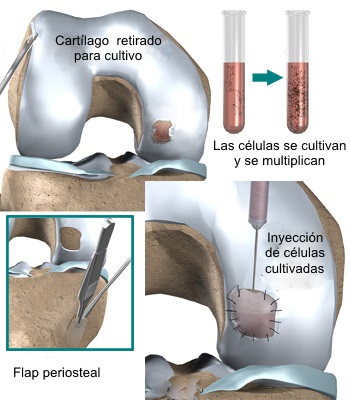
Implante
de condrocitos o células mesenquimales autólogas cultivadas.
Este tratamiento supone una nueva perspectiva en la reparación del
cartílago articular. Hasta el momento actual, este tipo de
tratamiento, basado en el aislamiento, cultivo y posterior
implantación de condrocitos autólogos, permite reparar con éxito,
defectos articulares inferiores a los 10 cm2. de superficie y cuya
profundidad puede llegar incluso hasta la placa subcondral. Sus
indicaciones principales serían pues los defectos en zona de carga,
de espesor completo y entre 4 cm2 y 10 cm2. Previamente se hará una
valoración artroscópica de la lesión, evaluándose la calidad de los
márgenes, la localización y el tamaño.
Existen series que tienen unos
resultados positivos del 90%, y además, las biopsias tomadas de
estos pacientes después de la cirugía muestran un cartílago hialino
similar al articular normal, sin embargo las lesiones que asientan
en el cartílago rotuliano son las que han demostrado una menor
respuesta clínica a este tipo de tratamiento, obteniendo los niveles
más bajos de satisfacción clínica.
En realidad, Se pueden cultivar condrocitos e implantarlos en la
articulación, pero realmente no se está reproduciendo la estructura
columnar del cartílago, no se sabe la calidad ni el nivel de
actividad y además no hay zonas de transición biomecánica.
Probablemente crezca un tejido de baja resistencia biomecánica y por
tanto se están creando áreas de dudosa longevidad real.
Factores
de crecimiento. Parece ser que los factores de
crecimiento actúan directamente sobre los condroblastos, mediante
unos receptores de superficie llamados integrinas e indirectamente
mediante modificaciones de la matriz extracelular que modulan las
señales transmitidas a las células desde la matriz extracelular. Son
factores de crecimiento con capacidad de promover el relleno de
defectos condrales con tejido rico en colágeno tipo 2, la proteína
morfogenética 2 recombinante humana (rhBMP-2) y el factor
transformador de fibroblastos beta (TGF-β).
Matrices
sintéticas. Estas matrices pueden estar formadas por
colágeno, fibras de carbono, geles de glucosaminglicanos y otros
materiales. Estas matrices proporcionan un entramado que favorece la
migración de células que utilizan dicha matriz para crear tejido
cartilaginoso. El uso de estas matrices se podría combinar con
condroblastos o células mesenquimales obtenidas en cultivo o con
factores de crecimiento.
Transplantes e implantes de tejido
cartilaginoso
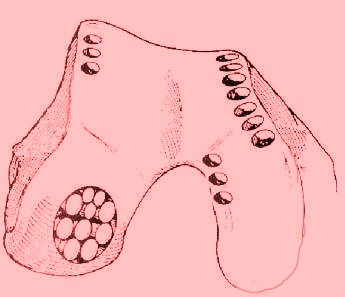
Autoinjerto osteocondral (Mosaicoplastia). Esta
técnica fue descrita por Matsusue et al. en 1993. La mosaicoplastia
es el trasplante de pequeños cilindros osteocondrales autólogos
procedentes de regiones de la articulación no sometidas a carga,
hacia una lesión condral u osteocondral en zona de carga. El
diámetro de estos cilindros oscila entre 2.7 y 4.5 mm. Su
implantación se asemeja a la forma de un "mosaico" y puede rellenar
de un 60% a un 80% de la superficie de la lesión. Está indicado en
lesiones de entre 2 y 6 cm2 así como en la fijación de
osteocondritis disecantes. Clínicamente los resultados son similares
a los del transplante autólogo de condrocitos, pero parece ser que
son mas prometedores desde el punto de vista histológico.
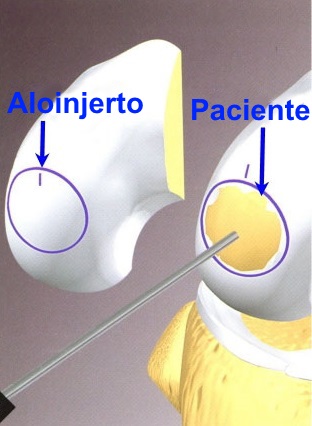
Aloinjerto osteocondral fresco y congelado. El
atractivo de esta técnica reside en que permite cubrir defectos
grandes con tejido cartilaginoso maduro en una sola intervención y
sin tener que lesionar zonas donantes sanas, y además permite la
conservación de la unidad funcional cartílago hialino-hueso
subcondral que garantiza un comportamiento biomecánico óptimo a la
vez que asegura una buena consolidación del injerto al lecho
receptor. El cartílago es casi avascular y se nutren por el líquido
sinovial por lo que los condrocitos están protegidos del sistema
inmune por la matriz circundante, con lo que el peligro de rechazo
está disminuido. Los aloinjertos frescos proporcionan mejor tejido
de reparación, debido a que incluyen condrocitos viables y permiten
una mejor revascularización ósea, pero por otro lado tiene el
inconveniente de que hay que hacer espera la cirugía hasta la
disponibilidad de tejido donante y por otro lado la posibilidad de
transmisión de enfermedades contagiosas. En cambio con el cartílago
congelado se disminuye la inmunogenecidad y permite mantenerlo
almacenado hasta su utilización, pero su integración es peor.
Implantes
de cartílago. Se ha conseguido desarrollar en el
laboratorio cartílago hialino por medio de diferentes sustratos. El
mas prometedor consiste en cilindros de metal trabecular sobre el
que puede cultivarse una capa de cartílago. Este metal se integra
muy bien en el tejido óseo y cartilaginoso, por lo que tiene buenas
expectativas en cuanto a la fijación y a la duración del implante.
Pero esta técnica está en aún en fase experimental.
|